Trump desata la guerra médico-comercial por el Remdesivir
La pandemia provocada por el covid-19 está desatando una guerra médico-comercial por el control de medicamentos y vacunas en la que el presidente Donald Trump vuelve a ser protagonista al comprar el 90% del medicamento Remdesivir, el que da en estos momentos mejores resultados para aplacar el covid-19.
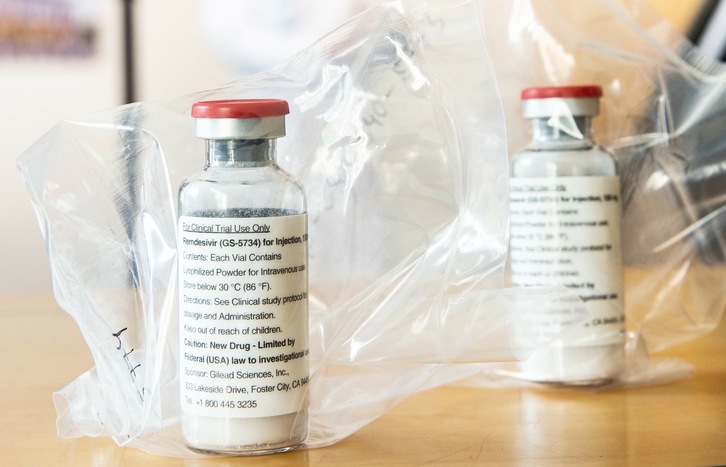
La prepotencia del presidente de EE.UU Donald Trump está desatando una velada guerra médico-comercial por el medicamento Remdesivir. Ha acaparado la producción de julio y el 90% de agosto y setiembre. Según el Departamento de Salud de EE.UU, han asegurado 500.000 tratamientos de Remdesivir.
Aunque desde la Unión Europea se asegura que está garantizado su suministro, se extienden las incógnitas ante la falta de nuevos medicamentos sustitutivos antes de que lleguen las vacunas que, como muy pronto, no lo harán hasta diciembre de este año.
Mientras tanto el covid-19 sigue extendiéndose por el mundo con más de 10,8 millones de afectados y casi 600.000 muertes.
¿Qué es?
Remdesivir es un antiviral diseñado en los laboratorios Gilead Sciencies, ubicada en San Francisco, California, para afrontar el ébola en 2013 y que se probó con virus de procedencia animal anteriores que no terminaron en pandemia. Cobra especial importancia cuando a finales de junio, por primera vez, la Agencia Europea del Medicamenteo (EMA) autorizó su comercialización para el tratamiento del covid-19 en adultos y adolescentes de más de 12 años con neumonía.
Su función fundamental es que ralentiza la producción de nuevas partículas de virus y, como resultado, la infección viral se desarrolla con menos rapidez y los pacientes en estado grave se recuperan una media de cuatro días antes de lo habitual. Así evita que el virus SARS-CoV-2 haga copias de sí mismo.
De todas maneras, no todos los científicos le atribuyen la eficacia que la empresa productora destaca, pero la realidad es que es de los pocos tratamientos médicos en estos momentos que han hecho retroceder al covid-19, si bien no en todos los casos.
La realidad es que, como se suponía, la farmaceútica ha experimentado un crecimiento importante en la bolsa financiera ante la enorme demanda que se prepara.
Controversia internacional
La decisión de Trump, que negoció con Gilead Sciencies ese acaparamiento del medicamento, ha generado una controversia global, lo que ha obligado a la Unión Europea y otros países a confirmar que hay Remdesivir asegurado, aunque más bien lo que están esperando es que no se desate de nuevo lo peor de la pandemia, como ocurrió entre marzo y finales de mayo, porque es evidente que su producción cubriría la demanda.
La Comisión Europea ha confirmado este jueves que está negociando con Gilead Sciences la reserva de viales de Remdesivir. «La Comisión también está actualmente en negociaciones con Gilead sobre la posibilidad de reservar dosis de remdesivir para los Estados miembros», ha expresado el portavoz de Salud del Ejecutivo comunitario, Stefan De Keersmaecker.
Ha rehusado dar más detalles sobre estas negociaciones por razones de confidencialidad, pero sí ha detallado que Washington no comunicó a la UE su acuerdo con la farmacéutica y, por tanto, las autoridades europeas se enteraron del mismo a través de la prensa. De hecho, Bruselas pretende, además, acelerar el proceso de autorización de este fármaco, algo que espera para «los próximos días», después de que la Agencia Europea del Medicamento (EMA) recomendara la semana pasada autorizar la comercialización del antiviral en la UE.
De Keersmaecker ha preferido no entrar en el detalle de cuántos viales y a qué precio desea pactar con Gilead para la compra de remdesivir, pero ha señalado que en la cuantificación de los mismos se tendrán en cuenta las necesidades de los hospitales europeos, tanto en la actualidad como las previstas para el futuro.
Gilead Sciences fijó en 390 dólares (347 euros) el precio de cada vial de Remdesivir, por lo que un tratamiento de cinco días con seis viales ascendería a 2.340 dólares (2.083 euros).
El Estado español cuenta con suficientes existencias de Remdesivir para tratar a pacientes graves hasta el próximo mes de octubre, momento en que la compañía que fabrica este fármaco tendrá ya disponibles nuevas dosis del tratamiento.
Así lo ha confirmado la directora de la Agencia Española de Medicamentos y Productos Sanitarios (Aemps), María Jesús Lamas, tras conocerse que EE.UU ha comprado casi todas las existencias de este medicamento.
Murga: «Garantizado en este momento»
Mientras, la consejera de Salud de la CAV, Nekane Murga, ha asegurado este jueves que en Araba, Bizkaia y Gipuzkoa se hace un uso limitado de Remdesivir y que su suministro «en este momento» está «garantizado».
Murga ha explicado que en la CAV este medicamento solo está indicado en ensayos clínicos sobre la covid-19 o para su «uso compasivo», es decir cuando «no hay alternativa terapéutica y se puede obtener un beneficio similar al de participar en un ensayo».
La realidad es que también Corea del Sur comenzó ayer a hacer uso del antiviral Remdesivir. El Centro de Control y Prevención de Enfermedades (KCDC) del país ha indicado que el medicamento desarrollado por la farmacéutica estadounidense Gilead será utilizado para el tratamiento de aquellos pacientes que presenten síntomas graves. Y confirmó que Gilead ha donado ya el primer lote, lo que ha abierto la puerta a futuras adquisiciones en el mes de julio, si bien los detalles sobre la cantidad a importar y el precio de la misma no han salido a la luz.
Un fármaco 'in vitro'
Se está librando una lucha por el control del mercado farmacéutivo frente al covid-19. De hecho, hoy se ha conocido que PharmaMar ha anunciado que su socio en Corea del Sur, Boryung Pharmaceutical, ha presentado los primeros resultados de los estudios «in vitro» de ‘Aplidin'’(plitidepsin) en SARS-CoV-2, el virus que provoca el covid-19, donde se observa una actividad antiviral hasta 80 veces mayor que el Remdesivir.
Según los datos de la actividad antiviral obtenidos en el estudio en el modelo de célula de riñón de mono, plitidepsina ha mostrado una actividad antiviral entre 2.400 y 2.800 veces mayor que Remdesivir (aprobado como medicamento para tratar los efectos graves), y también una actividad 80 veces mayor que el Remdesivir en el modelo de célula de pulmón humano.
Con estos datos de actividad antiviral, la compañía espera reducir la progresión de la enfermedad a un síndrome de distrés respiratorio agudo (SDRA) en los pacientes hospitalizados con neumonía por covid-19, junto con una rápida mejoría de los síntomas.
Boryung Pharmaceutical ha anunciado que ya están preparando los ensayos clínicos con plitidepsina en Corea y tiene como objetivo comenzarlos en el tercer trimestre de 2020. En abril, PharmaMar anunció el inicio del ensayo clínico con plitidepsina para el tratamiento de pacientes con COVID-19 en el Estado español.
En 2016, PharmaMar y Boryung Pharmaceutical firmaron un acuerdo de licencia para comercializar el fármaco antitumoral de origen marino, plitidepsina, en Corea del Sur. Según los términos del acuerdo, PharmaMar conserva los derechos exclusivos de producción y suministra el producto terminado a Boryung Pharmaceutical para su uso comercial.

La exposición temprana a pantallas se relaciona con cambios cerebrales en la adolescencia

Preparándose para confirmar en las urnas la anomalía vasca

Muere un joven motorista de 24 años en un accidente de tráfico en Hernani

El cantante estadounidense y exmarine Zach Bryan se casa en la Parte Vieja donostiarra
