Un brote en Erro reafirma la urgencia de la vacunación
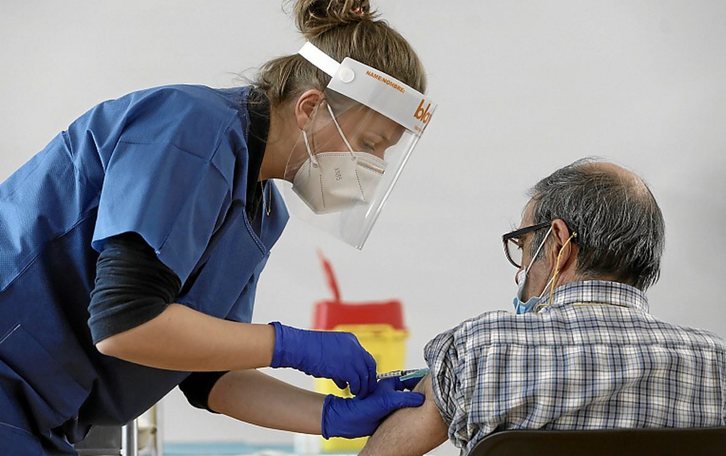
El Departamento de Derechos Sociales del Gobierno de Iruñea informó ayer de que se ha detectado un brote de covid en la residencia de mayores Ibañeta, en Erro, que afecta a 17 residentes. Tras el cribado a las 55 personas que residen en el centro, una de las afectadas ha sido trasladada a un recurso intermedio, mientras las otras 16 permanecerán aisladas en la residencia. Según indicó el Ejecutivo, todas estas personas habían recibido la primera dosis de la vacuna hace una semana, el 5 de enero.
A este respecto, el jefe de la Sección de enfermedades Transmisibles y Vacunaciones del Instituto de Salud Pública y Laboral de Nafarroa (ISPLN), Aurelio Barricarte, recordó que la vacuna que se está inoculando consta de dos dosis, por lo que, apuntó, «no son personas que se puedan considerar vacunadas».
«La protección, en un porcentaje cercano al 95% de la población inmunizada, se alcanza una semana después de la segunda dosis, por lo que este brote no debe extrañarnos», destacó Barricarte.
Preguntado sobre si las personas que han recibido la primera dosis cursarán la enfermedad en grado más leve, explicó que «la respuesta inmunitaria a la primera dosis tarda en producirse unos 14 días», de modo que como estas personas fueron vacunadas el día 5 «no ha habido tiempo suficiente para que hayan desarrollado dicha respuesta, y por tanto la enfermedad seguirá su evolución natural». Precisamente, este hecho lo que hace es reafirmar la necesidad de que todo el proceso de vacunación se lleve a cabo cuanto antes, sobre todo en los colectivos más vulnerables.
En este sentido, el Ejecutivo recordó que está previsto que dentro de ocho días, el 21 de enero, concluya la dispensación de la primera dosis en todo el ámbito sociosanitario y que el 12 de febrero finalice el proceso en ese colectivo.
En febrero, tres vacunas
Es probable que antes de que eso ocurra las autoridades sanitarias de Euskal Herria dispongan ya de tres vacunas distintas.
A la de Pfizer-BioNTech, que es la que se está administrando desde finales de diciembre, esta misma semana se le va a sumar la vacuna de Moderna, que recibió el visto bueno de la Comisión Europea la semana pasada.
Y ayer, la farmacéutica AstraZeneca y la Universidad de Oxford solicitaron a la Agencia Europea del Medicamento (EMA) una licencia condicional de uso de la vacuna en la Unión Europea, algo que le organismo regulador podría evaluar antes del 29 de enero. Según confirmó la agencia, sus expertos en medicamentos humanos (CHMP) analizarán el paquete de datos disponible en un «plazo de tiempo lo más breve posible».

ETA reconoce el daño causado en una «declaración solemne»

Abecedario de una campaña con grandes titulares y letra pequeña

EH Bildu vence con solvencia en el escenario del duelo más enconado

Salto histórico de EH Bildu y apuros para un PNV que dependerá del PSE

